
Un dosage permet de connaître la concentration d’une espèce en solution.
Un titrage est un dosage faisant intervenir une transformation chimique rapide et totale.
Lors d’un titrage colorimétrique un changement de couleur intervient.
Dans un titrage on a :
- un réactif titrant, dont on connaît la concentration
- un réactif titré de concentration inconnue.
Le montage classique d’un titrage :
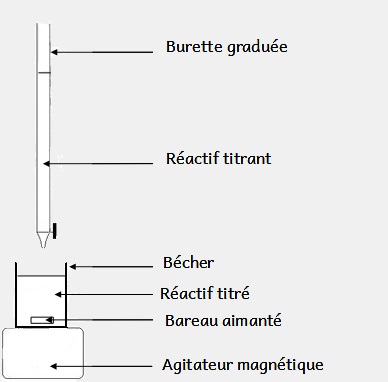
Remarque :
- le réactif titré est dans un bécher ou un erlenmeyer.
- le réactif titrant est dans une burette graduée.
Soit une réaction de titrage :
aA + bB → cC + dD
Lors d’un titrage le réactif titrant est ajouté jusqu’à ce qu’il soit en excès, c’est à dire que tout le réactif titré a réagit.
À l’équivalence la quantité de matière des réactifs est nulle.
Les réactifs ont été introduits dans les proportions stœchiométriques et la relation suivante est vérifiée :
=
Exemple :
Soit la réaction de titrage suivante :
2 S2O3 (aq)2 - + I2(aq) → S4O6 (aq) 2- + 2 I- (aq)
On souhaite titrer une solution de diiode I2(aq) à l’aide d’une solution d’ion thiosulfate S2O3 (aq)2 -.
Avant l’équivalence les ions thiosulfate sont en défaut (réactif limitant).
À l’équivalence on a où no(I2) est la quantité de diiode à doser et néq(S2O3 (aq)2 -) est la quantité de thiosulfate introduite à l’équivalence.
Quand on connaît la quantité de matière en diiode de l’échantillon, on peut déterminer la concentration de la solution de diiode.
Après l’équivalence les ions thiosulfate sont en excès, les ion I2(aq) sont en défaut.
Remarque :
Avant l’équivalence le réactif limitant est le réactif titrant.
Après l’équivalence le réactif limitant est le réactif titré.
À l’équivalence on change de réactif limitant.
Dans un titrage colorimétrique l’équivalence est repérée par un changement de couleur, par exemple avec le titrage suivant :
2 S2O3 (aq)2 - + I2(aq) → S4O6 (aq) 2- + 2 I- (aq)
incolore jaune incolore incolore
Au début on a :
- une solution incolore dans la burette
- une solution jaune dans le bécher
Au cours du titrage la solution du bécher se décolore progressivement jusqu’à devenir totalement incolore.
Pour un titrage on procède en deux fois :
- un premier titrage rapide (mL par mL) pour repérer la zone du volume équivalent Véq
- un deuxième titrage précis, on verse rapidement Véq – 2 mL de réactif puis on ajoute au goutte à goutte jusqu’au changement de couleur
QCM d'entraînement
lien vers le manuel
Exercices
QCM p 71
4, 5 p 73
7, 10 p 74
12 p 75