
Si deux atomes ont le même nombre de protons alors c’est le même éléments chimique.
Par exemple un atome dont le noyau a 2 protons c'est de l’hélium, si le noyau possède 6 protons c’est du carbone.
Si deux atomes ont le même nombre de protons mais un nombre de neutrons différents alors se sont des isotopes.
Deux isotopes ont donc le même numéro atomiques mais un nombre de masse différent.
Deux isotopes ont presque les mêmes propriétés chimiques et physiques, mais pour un même élément un isotope peut être stable dans le temps et un autre radioactif, c’est à dire qu’il va se désintégrer.
Exemple :
Le carbone peut exister sous forme de carbone 12 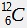 stable et de carbone 14
stable et de carbone 14 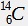 radioactif.
radioactif.
Remarque :
Cette radioactivité est naturelle, étant peu concentrée elle est peu dangereuse.
Lors d’une transformation nucléaire on passe d’un élément à un autre : c’est la transmutation.
Il y a conservation du nombre de nucléons et de la charge électrique mais la masse des réactifs est supérieure à la masse des produits : cette masse manquante est devenue de l’énergie c’est une réaction exothermique.
La quantité d’énergie obtenue est donnée par la formule suivante :
E = Δmc²
Avec :
E l’énergie en joule
Δm la différence de masse en kilogramme
c la vitesse de la lumière dans le vide en mètre par seconde
Au cours d’un fission nucléaire suite à l’impact d’un neutron un atome lourd va se séparer en deux atomes plus légers.
C’est la réaction qui a lieu dans les centrales nucléaires.
Exemple :
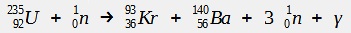
Avec γ le rayonnement gamma
Au cours d’un fusion nucléaire 2 atomes légers vont former un atome plus lourd.
C’est la réaction qui a lieu au cœur des étoiles.
Pour une même masse de réactif la fusion dégage beaucoup d’énergie que la fission.
Exemple de fusion :
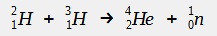
lien vers le manuel
Exercices :
QCM p 152
14, 18 p 153
21 p 154
25 p 155