
En chimie une synthèse permet de fabriquer en laboratoire une molécule existant dans la nature ou une nouvelle molécule.
Pour prélever un solide on mesure sa masse.
Pour prélever un liquide on mesure son volume.
Pour réaliser une transformation on utilise des montages, par exemple le montage à reflux :
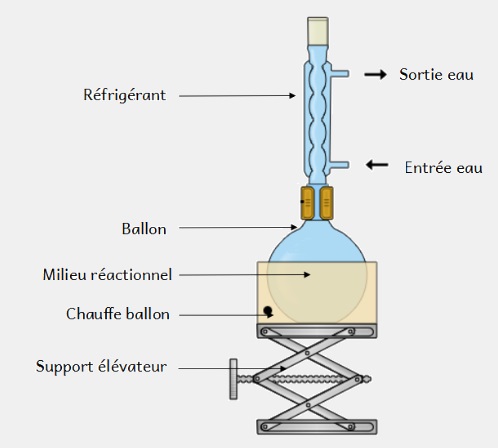
Ce montage permet d’accélérer les réactions, grâce au chauffage, tout en évitant les pertes de matières dû à la vaporisation.
Une fois la réaction fini on doit extraire le produit du milieu réactionnel.
Si le produit est une solide on peut l’isoler par filtration.
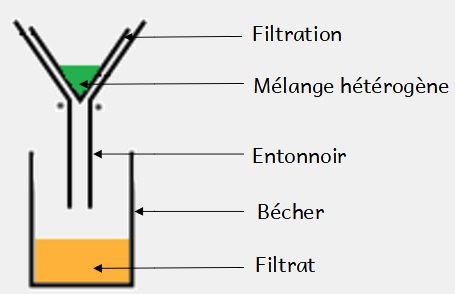
Puis on sèche le produit soit en étuve (chaleur) soit sous pression réduite.
Si le produit est liquide on peut l’isoler grâce à une ampoule à décanter. (voir chapitre 6)
Le produit sera toujours dans la phase où il est le plus soluble.
Parfois le produit formé contient des impuretés, il existe plusieurs techniques pour le purifier comme par exemple la distillation.
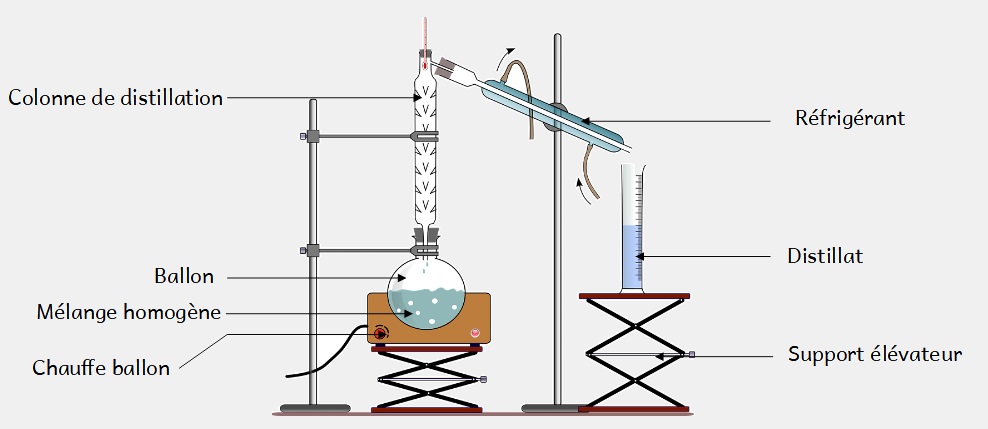
Une fois le produit isolé et purifié on procède à son analyse pour vérifier que l’on a bien formé le bon produit.
Pour cela on peut utiliser la CCM , l’analyse par infra-rouge ou pour les solides la mesure du point de fusion et les liquides la température d’ébullition.
Le rendement, noté η, est le rapport entre la quantité de matière en mole théorique nth de produit (celle que l’on aurai dû avoir) et la quantité expérimentale nexp (celle que l’on a obtenue), soit :
η =
Exemple :
Soit la réaction suivante :
C6H7NO + C4H6O3 → C8H9O2N + C2H4O2
On introduit 2 mol de C6H7NO et 4 mol de C4H6O3.
1) Quel est le réactif limitant ?
2) En théorie combien de produit C8H9NO2 peut-on obtenir ?
3) En réalisant la synthèse on obtient 1,5 mol de C8H9NO2.
Quel est le rendement de la synthèse ?
Correction :
1) Le réactif limant est le C6H7NO
2) En théorie on peut obtenir au maximum 2 moles de C8H9NO2.
3) Le rendement est de 0,75 soit 75 %.
lien vers le manuel
Exercices
QCM p 145
7 p 148
18 p150
21 p 151